发布时间: 2019-01-03 11:30:33
修改时间: 2019-01-03 11:53:54
阅读量: 5391
作者: 番茄
硝酸是一种具有强氧化性、腐蚀性的强酸。化学式:HNO3。熔点:-42℃,沸点:78℃,易溶于水,常温下纯硝酸溶液无色透明。
一、教学目标
(一)学习与目标
1.使学生掌握硝酸的物理性质和化学性质。
2.使学生了解硝酸的用途。
3.结合硝酸的浓度与它的氧化性的关系,阐明量变与质变的辩证关系。
4.通过演示实验之后废液、废气的处理,增强学生的环保意识。
(二)知识与技能:
1.使学生认识硝酸的易挥发性,区分纯硝酸、浓硝酸、“发烟”硝酸。
2.掌握硝酸的不稳定性和强氧化性。
3.认识硝酸的浓度与它的氧化性的关系。
4.掌握三大强酸的性质,认识它们性质的异同。了解硝酸在工业上的重要应用。
(三)情感与价值
1.通过对教材实验的改进,培养学生的实验创新设计能力。
2.通过演示实验,培养学生的实验观察能力、分析能力。
3.使学生逐步形成学习新知识,探究新问题的科学方法。
二、教学重、难点
1.教学重点:硝酸的氧化性
2.教学难点:硝酸的氧化性;实验设计的合理性、科学性及成功的可能性。
三、教学方法
启发探究、分组实验、电脑幻灯投影显示。
四、教具
电脑、 投影仪、实验用具及有关化学试剂。
五、教学过程
(一)引入
1.引入:幻灯片故事《玻尔巧藏诺贝尔金质奖章》
2.设计意图:对学生进行爱国主义教育。激发学生兴趣。
(二)指导探究
1.每两人一组,进行观色态,闻气味;打盖观雾;与水混合。
2.由一名学生综合概括,得出结论:纯硝酸是无色、易挥发、有刺激性气味的液体,溶于水。
(三)设疑过度
1.为什么久置的浓硝酸呈黄色?这与硝酸的化学性质有关
2.用方程式表示
酸的通性:
与碱反应
与碱性氧化物反应
动手实验:硝酸滴到紫色石蕊试纸上;铝加入到浓硝酸中
3.培养推理能力并在共性中发现问题。
(四)引导分析
1.HNO3中N显“+5”价,产物NO2中N 显“+4”价,由氧化还原反应的实质推断可能的产物。
2.培养学生由现象推结论的能力。
3.培养分析推理能力。
(五)引导总结
1.浓硝酸、稀硝酸与铜的作用的不同点。
2.学生总结:①浓硝酸生成NO2、稀硝酸生成NO气体。浓硝酸反应快,不需加热,稀硝酸反应慢,有时需要加热。
教师归纳:HNO3无论浓稀都有强氧化性与不活泼金属反应时主要是HNO3中“+5”价N得到电子,浓HNO3被还原成NO2气体,稀HNO3被还原成NO气体。浓HNO3氧化性更强。
2.提出问题:实验室能否用稀硝酸与锌粒制取氢气?为什么呢?
(六)课外探究
及时反馈,利教利学、知识总结,认识上的飞跃。
六、板书设计
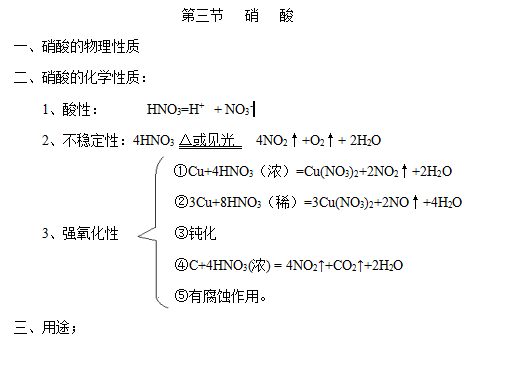
通过化学新课教学,引导学生从“不知”到“知”的认识过程,体现学生的主体性,面向全体学生,使学生感悟到知识的发生。
推荐阅读:
